Foszfin
Ebben a cikkben a Foszfin lenyűgöző világát fogjuk felfedezni, amely téma az évek során sokak figyelmét felkeltette. A Foszfin egy olyan koncepció, amely nagy vitákat és vitákat váltott ki különböző területeken, a tudománytól és a technológiától a populáris kultúráig és általában a társadalomig. Ha többet tudunk a Foszfin-ről, jobban megérthetjük annak életünkre és a minket körülvevő világra gyakorolt hatását. Ebben a cikkben a Foszfin különböző aspektusait fogjuk megvizsgálni, az eredetétől és fejlődésétől a jelenlegi és jövőbeli következményeiig. Készüljön fel a felfedezés és a Foszfin megismerésének útjára.
| Foszfin | |||
| |||
| |||
| IUPAC-név | Foszfán | ||
| Szabályos név | Foszfin | ||
| Más nevek | Foszfor-hidrogén | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 7803-51-2 | ||
| PubChem | 24404 | ||
| ChemSpider | 22814 | ||
| EINECS-szám | 232-260-8 | ||
| ChEBI | 30278 | ||
| RTECS szám | SY7525000 | ||
| InChIKey | XYFCBTPGUUZFHI-UHFFFAOYSA-N | ||
| Beilstein | 3600171 | ||
| Gmelin | 287 | ||
| UNII | FW6947296I | ||
| UN-szám | 2199 | ||
| ChEMBL | CHEMBL2227836 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | PH3 | ||
| Moláris tömeg | 34,00 g/mol | ||
| Megjelenés | színtelen gáz | ||
| Sűrűség | 1,5312 kg/m³ (0 °C, gáz)[1] 0,7653 g/cm³ (folyadékfázis, forrásponton)[1] | ||
| Olvadáspont | ‒133,80 °C[1] | ||
| Forráspont | ‒87,77 °C[1] | ||
| Oldhatóság (vízben) | 330 mg/l (20 °C)[1] | ||
| Kristályszerkezet | |||
| Molekulaforma | Trigonális piramis | ||
| Dipólusmomentum | 0,58 D | ||
| Veszélyek | |||
| EU osztályozás | Rendkívül gyúlékony (F+) Nagyon mérgező (T+) Veszélyes a környezetre (N)[2] | ||
| NFPA 704 | |||
| R mondatok | R12, R17, R26, R34, R50[2] | ||
| S mondatok | (S1/2), S28, S36/37, S45, S61, S63[2] | ||
| Öngyulladási hőmérséklet | 38 °C | ||
| Rokon vegyületek | |||
| Rokon vegyületek | Ammónia Arzin Sztibin Bizmutin Trimetilfoszfin Trifenilfoszfin | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A foszfin vagy foszfor-hidrogén egy szervetlen foszforvegyület, amelynek összegképlete PH3. Az ammóniáéhoz hasonló szerkezetű molekulákat alkot. Színtelen, kellemetlen szagú gáz. Vízben alig oldódik. Erősen redukáló hatású. Erős méreg.
Szerkezete
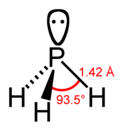
A foszfinmolekula az ammóniamolekulához hasonlóan trigonális piramis alakú. A központi foszforatomon egy nemkötő elektronpár van. A foszfin molekulájában a foszforatom nitrogénatomnál nagyobb atomsugara miatt jobban érvényesül a nemkötő elektronpár deformáló hatása, mint az ammóniában, ezért a kötésszög itt kisebb, 93,5°.
Kémiai tulajdonságai
A foszfin gyengén bázisos jellegű, hidrogén-halogenidek hatására foszfóniumsókká alakul. Azonban az ilyen PH+4-iont tartalmazó vegyületek sokkal bomlékonyabbak, mint az ammóniumsók. A foszfin hevítés hatására meggyullad és foszforsav képződése közben elég.
Klór hatására foszfor-pentakloriddá oxidálódik:
Előállítása
Foszfin keletkezik, ha fehérfoszfort erős lúggal főznek. Az így nyert foszfin azonban mellékterméket, difoszfánt (P2H4) tartalmaz. Ez a vegyület a levegőn magától meggyulladhat.
A foszfidokból (például kalcium-foszfidból) víz hatására szintén foszfin fejlődik.
Felhasználása
A foszfint kártevőirtásra használják, emellett alapanyag kémiai szintéziseknél.
Toxicitása
Belélegzése vagy bőrrel való érintkezés útján történő felszívódhat. Nagy dózisban halálos méreg. Tüdőödéma kialakulásához is vezethet a belélegzése. Mivel a foszfin nagyobb fajsúlyú, mint a levegő, ezért a talaj közelében megtelepszik. Emiatt fokozottan veszélyes a gyerekek egészségére. A szervezetbe, véráramba került foszfin a vér oxigénszállító képességét blokkolja és a sejtek oxigénfelvételét nehezíti meg.[3][4][5][6][3][7]
Belégzésének tünetei: rosszullét, hányás, hasmenés, hidegrázás, izomfájdalom, szomjúság, légzési nehézség, tüdőödéma. 50 ppm értéknél már rendkívül veszélyes az egészségre.[8]
Jegyzetek
- ↑ a b c d e A foszfin vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. január 24. (JavaScript szükséges) (angolul)
- ↑ a b c A foszfin (ESIS)[halott link]
- ↑ a b Two toddlers die after Jerusalem home sprayed for pests. Haaretz, 2014. január 22. (Hozzáférés: 2014. január 23.)
- ↑ rtve.es: "La familia de Alcalá de Guadaíra murió tras inhalar fosfina de unos tapones", 2014-02-03
- ↑ Deaths of Quebec women in Thailand may have been caused by pesticide. cbc.ca, 2014. március 13.
- ↑ „4 children killed after pesticide released toxic gas underneath their home, police say”, Washington Post (Hozzáférés: 2017. január 6.)
- ↑ Pesticide blamed in 8-month-old's death in Fort McMurray. CBC News, 2015. február 23. (Hozzáférés: 2015. február 23.)
- ↑ Ezért veszélyesek a Mátrai Erőműnél felbukkant gázok. Index.hu. (Hozzáférés: 2019. november 27.)
Források
- Nyilasi János: Szervetlen kémia
- Bodor Endre: Szervetlen kémia I.






